AZ ORVOSI KANNABISZ BIOHASZNOSULÁSA – MELYEK A LEGHATÉKONYABB FOGYASZTÁSI MÓDOK?
A meglévő gyógyászati kannabiszpiacon számos termék áll rendelkezésre, amelyek különféle beadási módokkal alkalmazhatók. A biohasznosulása az a mérték vagy sebesség, amellyel egy készítmény hatóanyaga felszívódik az egy elő rendszerbe vagy elérhetővé válik a fiziológiai aktivitás helyén, így ez az arány igen fontos a hatékonyság szempontjából. Annak érdekében, hogy egy gyógyszer működjön, el kell érnie a tervezett rendeltetési helyét. A terápiás vegyületek (ebben az esetben a CBD és a THC) beadási módja rendkívül fontos, mivel befolyásolhatja a szer felvételét, eloszlását és kiürülését, illetve ebből következik, hogy mennyire hatékony az orvosi kannabisz terápiás hatása.
A kannabinoidok sokféleképpen alkalmazhatók a felhasználó igényeinek és preferenciáinak megfelelően. Az orvosi gyakorlatban a felhasználó számára előnyös mód (mennyire kényelmes a szer bevétele) nagyon fontos tényező lehet, és gyakran nagy szerepet játszik az orvosságok felírásában is. Azonban a kényelmet nem szabad a hatékonyság szempontjából kiemelten kezelni, mivel az alkalmazás módja nagyobb hatással lehet a betegség kezelésére.
A biohasznosulás esetében gyógyszer véráramba jutását vizsgálják a szakemberek. A kutatások során abból indulnak ki, hogy az intravénásan beadott szerek biohasznosulása 100%, így a más beadási módok során százalékkal jelzik, hogy mekkora arányban (és milyen sebességgel) jut el a gyógyszer a kívánt helyre.
A biohasznosulás és az étkezés fontossága
Az orvosi kannabisz biohasznosulásának vizsgálata során mindenképpen beszélni kell egy tényezőről, amelyet ritkán emlegetnek a jelenséggel kapcsolatban, ez pedig az étkezés. A gyógyászati kannabisz alkalmazásakor lezajló biohasznosulással kapcsolatban fontos, hogy a szervezet egészséges zsírszinttel rendelkezzen, ugyan úgy, ahogy a zsírban oldódó vitaminok (A, D, E és K vitaminok) esetében. Azonban nem minden zsír ugyanaz. A két leghíresebb a telített zsírok és telítetlen zsírok. A telített zsírok a “rossz” koleszterinként ismert alacsony sűrűségű lipoproteinek (LDL), a telítetlen zsírok pedig a “jó” koleszterinként ismert nagy sűrűségű lipoproteinek (HDL).
Az LDL dolga az, hogy koleszterint biztosítson a sejteknek az egész testében, míg a HDL koleszterint von el szívtől és más szervektől, és visszaszállítja a májba. Ez fontos megkülönböztetés, mert amikor orvosi kannabisz fogyasztunk, akkor THC-t és a CBD-t igyekszünk a sejtekbe juttatni.
Egy tanulmány szerint THC-nak egyértelmű affinitása van az emberi plazma LDL-frakciójához (bár a tanulmány azt is kimutatta, hogy a THC kötődik HDL-hordozókhoz is, de nem annyira, mint az LDL-hordozókhoz). Tehát ne hagyjuk, hogy a “jó” és a “rossz” címkék félrevezessenek (ahogy korábban pl. a CBD-t “jónak” nevezték és a THC-t pedig “rossznak”, de az orvosi kannabisz felhasználási területei ennél azért sokkal szofisztikáltabbak).
Az egészséges LDL-értékű élelmiszerek: minden olyan szerves tejtermék, amely 2% feletti zsírtartalommal rendelkezik, tojás, nem nagyüzemi marhahús, bárány, sertés, csirke, hal, kagyló, kakaóvaja, pálmaolaj és a kókuszolaj.
Az orvosi kannabisz különféle bevételi módjainak biohasznosulása
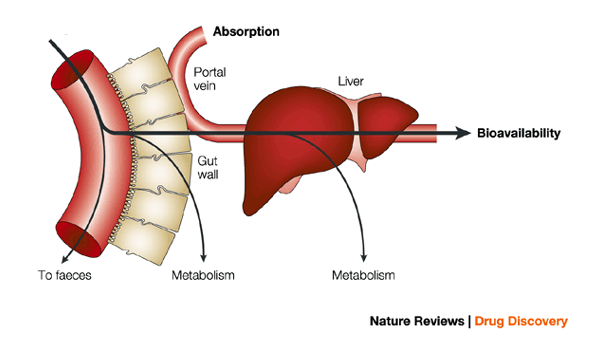
Az orvosi kannabisznak tehát többféle bevételi módjai vannak, vegyük sorra ezeket. Az első, és talán legelterjedtebb a szájon át való (orális) bevétel, amely azért is népszerű, mert a kannabinoidokat számos élelmiszertermékbe be lehet építeni, illetve kapszulákon vagy olajokon keresztül szintén könnyen alkalmazható. A lenyelt THC és CBD biohasznosulása 4% és 20% közötti értéket mutat, amelyek többsége az alacsonyabb tartományban van. Ennek oka az úgynevezett „first pass” metabolizmus, amelynek során a gyógyszer először a májba kerül, ahol jelentős hányada metabolizálódhat, azaz feldolgozásra kerül mielőtt még eljuthatna a szisztémás keringésbe, illetve a hatás helyére. Az orális fogyasztás előnye, hogy a hatóanyagok hatása 5-8 órán át tart, így a betegnek kell gyakran alkalmazni a szereket.
A rektális kúpok alkalmazása pozitív hatásokat mutat, a helyes alkalmazás esetén (ami a rectalis superior elkerülését jelenti), és megakadályozza a „first pass” anyagcserét.
Sajnos nagyon kevés tudományos vizsgálat áll rendelkezésre a rektális alkalmazás biohasznosulásáról. Egy majmokon végzett vizsgálat 13,5% biohasznosulást mutatott, azonban egy másik, két beteg által végzett vizsgálat szerint a biohasznosulás megközelítőleg kétszerese az orális bevételnek, de itt nem állnak rendelkezésre pontos százalékok.
Egy 2018-as kutatás tisztázni látszik a korábbi félreértéseket a raktális kúpok felszívódásáról, amik akár 80%-os biohasznosulást is igértek, az orális adagolással szemben. Ebben a vizsgálatban a ElSohly és csapata úgy találta, hogy a THC-HS* kúp rektális beadása után az delta-9-THC koncentrációja körülbelül 70-80%-ban biohasznosítható, ami majdnem 2.5-szer nagyobb, mint egy orálisan bevitt THC-kapszula esetében. Bár a vizsgálati alanyoknál nem számoltak be pszichotróp hatásokról, a kutatás azt állítja, hogy a first pass anyagcsere „nagymértékben csökkent”, bár nem szűnt meg teljesen. Ez azt jelenti, hogy a 11-hidroxi-THC némi kis pszichotróp hatása előfordulhat a THC-HS formuláció esetében, de további vizsgálatok szükségesek ennek megerősítéséhez.
ElSohly kutatásai jelentősen befolyásolhatják a rákos betegeket és másokat, akik olyan betegségekben szenvednek, amelyeknél nagyon nagy dózisú kannabinoidok szükségesek, de nem tudnak inhalálni (szívni) vagy szájon át adagolni. A THC-HS egy szabadalmaztatott molekula, és csak a Mississippi Egyetem engedélyével állítható elő.
(*A THC egy kémiailag módosított változata, amit THC-hemiszukcinátnak (vagy röviden THC-HS) neveznek, biológiai biológiailag hasznosul a végbélben. A szukcinát, egy közbenső vegyület a cukor lebontásában, enyhén vízoldható, ami lehetővé teszi, hogy felszívódjon a végbél nyálkahártyáján. Először az ElSohly Laboratories Inc. szintetizálta. A hagyományos THC-val ellentétben a hemisukcinát-észterből származó THC könnyen áthatol, és a rektális nyálkahártyákba szívódik fel. Ennek eredményeként a THC nagy része elkerüli a first pass anyagcserét, és nem alakult át a jóval pszichotrópabb hatású metabolitjává a májban, 11-hidroxi-THC-vá.)
A rektális kúpok 2-3 centiméter hosszúságúak és 2 gramm súlyúak. A végbélbe kerülnek (az utolsó 15-20 cm-es gyomor-bél traktusba), ahol 3 külön vénában is felszívódhatnak; az alsó, középső és felső rektális (haemorrhoidális) vénákban. Az alsó és a középső vénák közvetlenül a központi vérkeringésbe vezetnek, míg a felső csatorna (rectalis superior) közvetlenül a májba áramlik.
Számos fiziológiás tényező (a rendelkezésre álló folyadék mennyisége, a rektális folyadék tulajdonságai, a végbél tartalma, vagy a keringési útvonal) és a gyógyszerek fiziko-kémiai tulajdonságai (a hatóanyag oldhatósága a vivőanyagban, részecskeméret, a bázis jellege, elterjedési kapacitás) is hatással van a rektális felszívódásra.
Íme néhány példa a kannabinoid kúpok használatára:
- Aranyér, gombák
- Gyulladásos bélbetegség
- Daganatok (női, férfi)
- Hüvelykúp
A beszámolók szerint a nyelv alatti adagolás esetében szintén pozitív eredményeket tapasztaltak. Mivel azonban a nyelv alatt nyálmirigy található, a módszer reflexszerű nyeléshez vezethet, amely csökkenti a biohasznosulást és növeli a THC pszichoaktív hatását. Bár számos gyógyszer esetében léteznek kutatások az nyelv alatti bevételi módról, a THC és a CBD esetében nincsenek vizsgálatok a biohasznosulásról. A rendelkezésreálló adatok szerint a nyelv alatti adagolás biohasznosulása kicsit magasabb, mint az orális alkalmazásé. A szublingvális alkalmazás a második leggyorsabb módja a THC és a CBD testbe való bejuttatásának a dohányzás/inhalálás után.
Számos módja lehet az orális biohasznosulás növelésének. Egy nemrégiben készült tanulmány szerint a CBD és a hosszú szénláncú trigliceridek egyidejű alkalmazása segít elkerülni a „first pass” anyagcserét. Ilyen módon a kannabinoid a bélrendszer nyirokrendszerén keresztül, következésképpen a bal oldali belső jugularis és bal subclavia vénákon keresztül jut el a véráramba, és kikerüli a májat a folyamatban.
A bukkális (szájban tartandó)/szájnyálkahártyán történő adagolásról szóló beszámolók is jó eredményekről szóltak. A módszer előnyösebb, mint a szublingvális adagolás, mivel nincsenek reflexnyelések, így a gyógyszer a helyén marad. A GW Pharmaceuticals szerint: “A kannabinoidok esetében a felszívódási görbe alatti terület (AUC) hasonló a szublingvális és bukkális adagolás során.” A bukkális beadás után jelentősen csökkent a kannabinoidok primer (11-hidroxi-metabolitja) mennyisége. Ez megerősíti, hogy a kannabinoid/hatóanyag nagyobb arányban szívódik fel transzmukozálisan, mint a nyelv alatti adagolás esetében. Itt meg kell jegyezni, hogy a vizsgálatok során a THC és a CBD kivonatokat olyan segédanyagokkal keverték össze, mint az etanol, a propilénglikol és a borsmentaolaj.
Az elszívás vagy vaporizálás esetében szintén pozitív beszámolók születtek. Ez az adagolási mód is megakadályozza a „first pass” anyagcserét. Bár a vaporizálás egészségesebb, mint a dohányzás, a biohasznosulás szempontjából gyakorlatilag azonosak. Az elszívás és az inhalálás biohasznosulása a tapasztalt fogyasztóknál magasabb, mint az újaknál, így a haszonulás értékei 2% és 56% között változtak a különböző vizsgálatokban, a legtöbb eredmény azonban a magasabb tartományban volt. A THC és a CBD bejuttatásának ez a leggyorsabb módja, és az intravénás alkalmazás kivételével, az elszívás vagy a vaporizálás esetében mutatták ki a legmagasabb plazmacsúcsokat. Azonban a gyógyászati hatások 3 óránál rövidebb ideig tartanak, ami azt jelenti, hogy az betegeknek gyakrabban kell alkalmaznia a szert a folyamatos gyógyszeres állapot fenntartásához. Az elszívás/vaporizálás kiemelkedően hatékony, amelyre a kilégzés a bizonyíték: a kilélegzett gőz olyan kannabiszt tartalmaz, amely nem szívódott fel a tüdőben és a szervezet kidobta magából.
A krémek/balzsamok alkalmazása során a gyógyászati kannabisz interakcióba kerül a CB1 és a CB2 receptorokkal. Ezek a CB receptorok jelen vannak az egész testben, beleértve az izmokat, a bőrt, a csontokat, a perifériás idegeket és a szinoviális szöveteket. Tehát még akkor is, ha nem bizonyított a THC és a CBD a bőrön át történő bejutása a véráramba hordozók nélkül, a beszámolók azt sugallják, hogy a kannabisz hatóanyagai ezeken a területeken is kölcsönhatásba léphetnek a CB receptorokkal.
Konklúzió
A biohasznosulás szempontjából a szublingvális és belégzési útvonalak a leghatékonyabbak a hatóanyagok véráramba juttatásához. Ez fontos lehet olyan tünetek esetén, amelyek gyors enyhülést és magas hatóanyag-tartalmat igényelnek a véráramban.
Azonban nem létezik egyetlen, mindenhol és mindenki által használható, tökéletes megoldás, ahol egy módszer mindenben jobb, mint a többi. Az orális adagolás hatékony lehet a kényelem és a könnyűség szempontjából, valamint olyan tünetek kezelésére, amelyek kis koncentrációjú, hosszabb ideig tartó hatóanyagot igényelnek a szisztémás keringésben. A rektális beadás helyi gyulladáscsökkentő hatást eredményezhet, amely kulcsfontosságú a különböző vastagbélbetegségek kezelésében, valamint a nagyobb biohasznosulás révén a hatóanyagkoncentráció is magasabb a test célterületeinél.
Kiegészítés:
1) Úgy tűnik, hogy a THC biohasznosulása jobb, mint a CBD-é – Egy klinikai vizsgálat kannabiszalapú gyógyszerkivonatokat használt, és arra a következtetésre jutott, hogy “a THC biológiai hozzáférhetősége nagyobbnak mutatkozik, mint a CBD-é”. Egy másik klinikai vizsgálat azt találta, hogy miután a szublingvális, bukkális, oropharyngeális és orális módszerekkel 10 mg THC és CBD tartalmú kannabisz gyógyszerkészítményt adtak be, “a THC koncentrációja magasabb volt, mint a CBD megfelelő szintje a legtöbb időpontban.”
2) Transzdermálisan, a CBD jobban áthatol, mint a THC – Transzdermálisan (a bőrön átmenő) szempontból, egy tanulmány kimutatta, hogy a CBD 10-szer nagyobb áteresztőképességű, mint a THC.
3) Kókuszolaj a kedvelt olaj – Interneten sok helyen olvasható, hogy az orvosi kannabisz-közösségben a kókuszolajról olvashatók a legpozitívabb véleményeket, függetlenül attól, hogy éltelekről van szó vagy kannabiszkivonatokról. A kókuszolaj másik előnye a stabil kémiai szerkezet, amely sokkal hosszabb eltarthatóságot biztosít, mint más olajok.
4) A nanoemulzió potenciálisan nagymértékben megnöveli a kannabisz alapú ételek, spray-k és krémek biohasznosulását. A nanoemulziókat hosszú évek óta sikeresen alkalmazzák az élelmiszer-, kozmetikai-, gyógyszeripari és vegyipari ágazatokban. Mivel a kannabisz lipofil (hidrofób), a kannabisz szempontból a nanoemulzió legmeghatározóbb definíciója az, hogy egy finom olaj/víz diszperziót egy a 20-600 nm cseppméretű felületaktív anyag molekulaszerkezete stabilizál. A nanoemulzió a következő előnyöket kínálja a kannabisz ételek, spray-k és krémek biohasznosulásának potenciális növeléséhez:
– A liposzómák és a vesikulák helyettesítésére használható.
– Nem mérgező és nem irritáló.
– Jobb fizikai stabilitás.
– A nano méretű cseppek nagyobb felülete, nagyobb felszívódást biztosít.
– Különböző készítményekben használható, például habokban, krémekben, folyadékokban és spray-kben.
– Az olajban oldódó készítményeknek jobb felvételt biztosít a sejtkultúra-technológiában.
– Segíti a lipofil gyógyszerek oldódását.
Referenciák:
Abrams DI, Vizoso HP, Shade SB, Jay C, Kelly ME, Benowitz NL. Vaporization as a smokeless cannabis delivery system: a pilot study. Clin Pharmacol Ther. 2007 Nov;82(5):572-8.
Atsmon J, Cherniakov I, Izgelov D, Hoffman A, Domb AJ, Deutsch L, Deutsch F, Heffetz D, Sacks H. PTL401, a New Formulation Based on Pro-Nano Dispersion Technology, Improves Oral Cannabinoids Bioavailability in Healthy Volunteers. J Pharm Sci. 2018 May;107(5):1423-1429.
Brenneisen R, Egli A, Elsohly MA, Henn V, Spiess Y. The effect of orally and rectally administered delta 9-tetrahydrocannabinol on spasticity: a pilot study with 2 patients. Int J Clin Pharmacol Ther. 1996 Oct;34(10):446-52
Challapalli PV, Stinchcomb AL. In vitro experiment optimization for measuring tetrahydrocannabinol skin permeation. Int J Pharm. 2002 Jul 25;241(2):329-39.
Consroe P, Kennedy K, Schram K. Assay of plasma cannabidiol by capillary gas chromatography/ion trap mass spectroscopy following high-dose repeated daily oral administration in humans. Pharmacol Biochem Behav. 1991 Nov;40(3):517-22.
Elmes MW, Kaczocha M, Berger WT, Leung K, Ralph BP, Wang L, Sweeney JM, Miyauchi JT, Tsirka SE4, Ojima I, Deutsch DG. Fatty acid-binding proteins (FABPs) are intracellular carriers for Δ9-tetrahydrocannabinol (THC) and cannabidiol (CBD). J Biol Chem. 2015 Apr 3;290(14):8711-21.
ElSohly MA, Stanford DF, Harland EC, Hikal AH, Walker LA, Little TL Jr, Rider JN, Jones AB. Rectal bioavailability of delta-9-tetrahydrocannabinol from the hemisuccinate ester in monkeys. J Pharm Sci. 1991 Oct;80(10):942-5.
W. Guy, P. J. Robson. A Phase I, Double Blind, Three-Way Crossover Study to Assess the Pharmacokinetic Profile of Cannabis Based Medicine Extract (CBME) Administered Sublingually in Variant Cannabinoid Ratios in Normal Healthy Male Volunteers (GWPK0215) J Cannabis Ther 2003(3/4):079-120
W. Guy, P. J. Robson. A Phase I, Open Label, Four-Way Crossover Study to Compare the Pharmacokinetic Profiles of a Single Dose of 20 mg of a Cannabis Based Medicine Extract (CBME) Administered on 3 Different Areas of the Buccal Mucosa and to Investigate the Pharmacokinetics of of CBME per Oral in Healthy Male and Female Volunteers (GWPK0112) J Cannabis Ther 2003(3/4):079-120
Garrett ER, Hunt CA. Physiochemical properties, solubility, and protein binding of ∆9-tetrahydrocannabinol. J Pharm Sci. 1974; 63 (7): 1056-64
Grotenhermen, F. 2001. Harm reduction associated with inhalation and oral administration of cannabis and THC.
Gupta A, Eral HB, Hatton TA, Doyle PS. Nanoemulsions: formation, properties and applications. Soft Matter. 2016 Mar 21;12(11):2826-41.
Hollister LE, Gillespie HK, Ohlsson A, Lindgren JE, Wahlen A, Agurell S. Do plasma concentrations of delta 9-tetrahydrocannabinol reflect the degree of intoxication? J Clin Pharmacol. 1981 Aug-Sep;21(S1):171S-177S.
Huestis, M. A. 2007. Human Cannabinoid Pharmacokinetics. Chemistry & Biodiversity, 4(8), 1770–1804
Iain J McGilveray. 2005. Pharmacokinetics of Cannabinoids. Pain Research and Management, vol. 10, no. Suppl A, pp. 15A-22A
Jaiswal M, Dudhe R, Sharma P. K. Nanoemulsion: an advanced mode of drug delivery system. 3 Biotech. 2015 Apr; 5(2): 123–127.
Karschner EL, Darwin, Goodwin SR, Wright S, Huestis MA. Plasma Cannabinoid Pharmacokinetics following Controlled Oral delta-9-Tetrahydrocannabinol and Oromucosal Cannabis Extract Administration. Clinical Chemistry Jan 2011, 57 (1) 66-75;
Klausner HA, Wilcox HG, Dingell JV. The use of zonal ultracentrifugation in the investigation of the binding of delta9-tetrahydrocannabinol by plasma lipoproteins. Drug Metab Dispos. 1975 Jul-Aug;3(4):314-9.
Mannila J, Järvinen T, Järvinen K, Jarho P. Precipitation complexation method produces cannabidiol/beta-cyclodextrin inclusion complex suitable for sublingual administration of cannabidiol. J Pharm Sci. 2007 Feb;96(2):312-9.
Mattes RD, Shaw LM, Edling-Owens J, Engelman K, Elsohly MA. Bypassing the first-pass effect for the therapeutic use of cannabinoids. Pharmacol Biochem Behav. 1993 Mar;44(3):745-7
McGilveray IJ. Pharmacokinetics of cannabinoids. Pain Res Manag. 2005 Autumn;10 Suppl A:15A-22A.
Method for effecting systemic delivery of delta-9-tetrahydrocannabinol US 4933363 A
Munjal M, ElSohly MA, Repka MA. Chemical stabilization of a delta9-tetrahydrocannabinol prodrug in polymeric matrix systems produced by a hot-melt method: role of microenvironment pH. AAPS PharmSciTech. 2006;7(3):71.
Munjal M, Elsohly MA, Repka MA. Polymeric systems for amorphous delta9-tetrahydrocannabinol produced by a hot-melt method. Part II: effect of oxidation mechanisms and chemical interactions on stability. J Pharm Sci. 2006;95(11):2473–85.
Munjal M, Stodghill SP, Elsohly MA, Repka MA. Polymeric systems for amorphous delta 9-tetrahydrocannabinol produced by a hot-melt method. Part I: chemical and thermal stability during processing. J Pharm Sci. 2006;95(8):1841–53.
Ofem, O. W., Ogechukwu, O. E., Okeke, N. C., Ogoamaka, O. P., Amaechi, A. A., & Godswill, O. (2014). Some physical properties of novel Cannabis suppositories formulated with theobroma oil. African Journal of Pharmacy and Pharmacology, 8(44), 1127-1131.
Ohlsson A, Lindgren JE, Andersson S, Agurell S, Gillespie H, Hollister LE. Single-dose kinetics of deuterium-labelled cannabidiol in man after smoking and intravenous administration. Biomed Environ Mass Spectrom. 1986 Feb;13(2):77-83.
Ohlsson A, Lindgren JE, Wahlen A, Agurell S, Hollister LE, Gillespie HK. Plasma delta-9 tetrahydrocannabinol concentrations and clinical effects after oral and intravenous administration and smoking. Clin Pharmacol Ther. 1980 Sep;28(3):409-16.
Perlin E, Smith CG, Nichols AI, Almirez R, Flora KP, Cradock JC, Peck CC. Disposition and bioavailability of various formulations of tetrahydrocannabinol in the rhesus monkey. J Pharm Sci. 1985 Feb;74(2):171-4
Pharmaceutical formulations US7025992B2
Repka MA, ElSohly MA, Munjal M, Ross SA. Temperature stability and bioadhesive properties of delta9-tetrahydrocannabinol incorporated hydroxypropylcellulose polymer matrix systems. Drug Dev Ind Pharm. 2006;32(1):21–32.
Samara E, Bialer M, Mechoulam R. Pharmacokinetics of cannabidiol in dogs. Drug Metab Dispos. 1988 May-Jun;16(3):469-72.
Sampada B. Upadhye, Swapnil J. Kulkarni, Soumyajit Majumdar, Mitchell A. Avery, Waseem Gul, Mahmoud A. ElSohly, and Michael A. Repka. Preparation and Characterization of Inclusion Complexes of a Hemisuccinate Ester Prodrug of Δ9-Tetrahydrocannabinol with Modified Beta-Cyclodextrins. AAPS PharmSciTech. 2010 Jun; 11(2): 509–517
Schicho R, Storr M. Topical and systemic cannabidiol improves trinitrobenzene sulfonic acid colitis in mice. Pharmacology. 2012;89(3-4):149-55.
Stable suppository formulations effecting bioavailability of Δ9 -THC. US 5508037 A
Stinchcomb AL, Valiveti S, Hammell DC, Ramsey DR. Human skin permeation of Delta8-tetrahydrocannabinol, cannabidiol and cannabinol. J Pharm Pharmacol. 2004 Mar;56(3):291-7.
Susan L. Broom MA, Kenneth J. Sufka, Mahmoud A. Elsohly & Samir A. Ross. Analgesic and Reinforcing Properties of Δ-9-THC-Hemisuccinate in Adjuvant-Arthritic Rats. Journal of Cannabis Therapeutics, 1(3-4), June 2001
Valiveti S, Hammell DC, Earles DC, Stinchcomb AL. In vitro/in vivo correlation studies for transdermal delta 8-THC development. J Pharm Sci. 2004 May;93(5):1154-64.
Yu H1, Huang Q. Improving the oral bioavailability of curcumin using novel organogel-based nanoemulsions. J Agric Food Chem. 2012 May 30;60(21):5373-9.
Forrás:
https://orvosikannabisz.com/tamogatas/
Webshopunkban további termékek, leírások várják!